欧盟eCTD的历史沿革与强zhi实施欧盟自2003年逐步推进eCTD(电子通用技术文档)的标准化进程,初要求yao注册申请(MAA)采用CTD格式。2010年,集中审评程序(CP)率先强zhi使用eCTD,随后分散程序(DCP)和互认程序(MRP)分别于2015年、2017年跟进。至2019年,欧盟要求所有guo家程序(NP)的注册申请均以eCTD格式提交,标志着其电子递交体系的成熟。2024年,EMA启动,旨在提升技术兼容性与审评效率。eCTD验证标准的迭代与关键更欧盟的验证标准历经多次调整,例如2025年3月启用的,对文件结构、元数据和内容完整性提出更严格的要求。标准引入的“追踪表(TrackingTable)”强zhi校验规则(如)曾导致CEP(欧洲yao典适用性证shu)递交,后通过允许占位文件临时解决。与早期版本相比,,并细化了对PDF书签、超链接的规范性检查。瑞士eCTD注册咨询相关技术支持。浦东新区ANDAeCTD服务价格
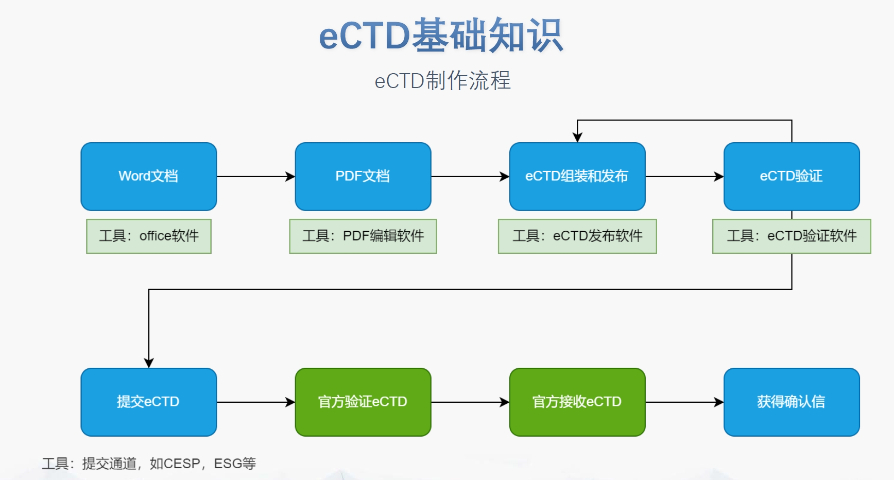
欧盟eCTD的递交途径与技术要求不同审评程序对应不同递交渠道:集中程序(CP)通过EMA的eSubmissionGateway或WebClient提交,分散程序(DCP)和互认程序(MRP)则需使用欧盟通用提交门户(CESP)。文件结构需严格遵循模块化要求,例如CEP申请需包含模块1(行政文件)、模块2(质量概述)和模块3(技术文档),且XML主干文件须符合EDQM的特定命名规则。此外,所有PDF文件需无密码保护、可全文检索,并嵌入层级书签以支持快su审阅。CEP申请的eCTD递交特殊性CEP程序自2018年起强zhi采用eCTD格式,重点评估原料yao是否符合欧洲yao典标准。其模块1需包含EDQM申请表、简历及变更说明表,模块2需使用EDQM提供的质量概述模板,模块3则按CTD格式组zhi。CEP与ASMF(活性物质主文件)的主要区别在于性:CEP无需关联上市许可,且审评由EDQM完成。山东化学药品eCTD递交美国eCTD申报软件相关技术支持。
欧洲YAO品管理局:集中审评程序由欧洲YAO品管理局(EuropeanMedicinesAgency,EMA)负责协调。人用YAO品委YUAN会:人用YAO品委YUAN会(CommitteeforMedicinalProductsforHumanUse,CHMP)负责提供科学意见。欧盟委员会:CHMP的意见随后被提交给欧盟委YUAN会(EuropeanCommission,EC),由欧盟委会做出是否授权的终决定。这个决定在整个欧盟都是具有法律约束力的。审批过程:申请人向EMA提交申请,包括eCTD(电子通用技术文档)格式的YAO品注册文档。EMA的CHMP分配一个科学评估团队(Rapporteur和Co-Rapporteur),负责初步评估。CHMP基于评估团队的报告提供科学意见。欧盟委会根据CHMP的意见做出终决定,批准或拒绝YAO品上市。授权范围如果YAO品获得批准,将获得在整个欧盟、冰岛、列支敦士登和挪威YOU效的上市许可(CentralMarketingAuthorisation,CMA)。
美国药物主文件(Drug Master File, DMF)是向FDA提交的机密技术文件,用于支持药品生产、质量控制及合规性审查。以下为申报的要点和流程总结: DMF概述与类型 定义与作用 DMF是药品生产全过程的详细档案,包含原料药、辅料、包装材料等的生产设施、工艺、质量控制等信息,供制剂厂商引用以支持其注册申请。其意义在于保护企业机密的同时,满足FDA对供应链透明度的要求。 DMF类型 Ⅱ类:原料药、中间体及制剂(如微生物外泌体、细胞株等生物制品均属此类)。 Ⅲ类:包装材料。 Ⅳ类:辅料、着色剂等添加剂。 Ⅴ类:非临床/临床数据等特殊信息(需FDA预先批准)。 注:Ⅰ型(生产设施与人员)已于2000年停用。欧盟eCTD申报软件相关技术支持。
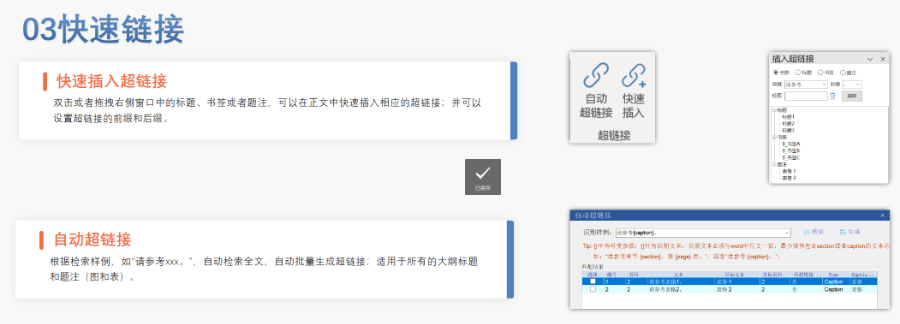
eCTD的技术架构与模块要求:美国eCTD基于XML技术,严格遵循ICHM4框架,分为5个模块:模块1(地区行政信息)、模块2(技术总结)、模块3-5(质量、非临床与临床数据)。其中,模块1需包含FDA特定的,涵盖申请编号、联系人和DMF授权书等行政信息。模块2-5需与ICHCTD全球统一标准一致,但FDA对文件颗粒度要求更细,例如非临床研究报告需拆分并标记StudyID。PDF文件需符合FDA,包括字体嵌入、书签层级和超链接功能。eCTD的技术架构与模块要求:美国eCTD基于XML技术,严格遵循ICHM4框架,分为5个模块:模块1(地区行政信息)、模块2(技术总结)、模块3-5(质量、非临床与临床数据)。其中,模块1需包含FDA特定的,涵盖申请编号、联系人和DMF授权书等行政信息。模块2-5需与ICHCTD全球统一标准一致,但FDA对文件颗粒度要求更细,例如非临床研究报告需拆分并标记StudyID。PDF文件需符合FDA,包括字体嵌入、书签层级和超链接功能。 加拿大eCTD注册咨询相关技术支持。无锡赋悦科技eCTD供应商
eCTD申报相关技术支持。浦东新区ANDAeCTD服务价格
多国审评程序与eCTD递交途径的适配:欧盟yao品审评程序包括集中(CP)、分散(DCP)、互认(MRP)和guo家程序(NP),eCTD需适配不同程序的递交要求。例如:集中审评程序(CP):通过EMA的eSubmissionGateway提交,审评时限约240个工作日,eCTD需包含完整的模块1-5及多语言标签文件。分散审评程序(DCP):需通过CESP(欧盟共同提交门户)递交,参考成员国(RMS)主导审评,eCTD需支持多国同步评估的模块化拆分。互认程序(MRP):已授权成员国作为RMS,eCTD需包含基线序列(BaselineSequence0000)以整合历史审评数据,并通过CMDh协调分歧。浦东新区ANDAeCTD服务价格