鉴于医疗器械创新发展迅猛和全球化发展趋势,实施医疗器械临床试验前安全性评价GLP管理是大势所趋。国家药品监督管理局医疗器械技术审评中心已经成立了医疗器械动物实验研究相关指导原则起草制定工作组,正在陆续发布针对具体类别的临床前动物实验研究相关指导原则。中国食品药品检定研究院医疗器械检定所初步搭建了医疗器械临床前动物实验研究平台。相信医疗器械动物实验研究领域会很快建立起健全的规范管理体系,为国内医疗器械的创新发展和百姓的用械安全保驾护航。生物药临床前动物实验是什么?黑龙江专业临床前动物实验研究

医疗器械临床试验前动物试验研究,作为在临床试验之前初步验证医疗器械安全性及有效性的手段,对于尚没有大量临床应用历史的高风险医疗器械以及创新型医疗器械来说是必要的试验。我国在2016年3月23日发布了《医疗器械临床试验质量管理规范》,在该管理规范中,明确要求在临床试验研究之前申请者应当完成必要的动物试验研究以及风险分析。关于是否需要做临床前动物试验研究应根据产品的风险分析进行判断。2019年4月19日,国家药品监督管理局(NMPA)发布了《医疗器械动物实验研究技术审查指导原则***部分:决策原则》,对如何决策是否有必要进行临床前动物实验研究给出了指导性建议。宁夏专业临床前动物实验指标生物药临床前动物实验多少钱?
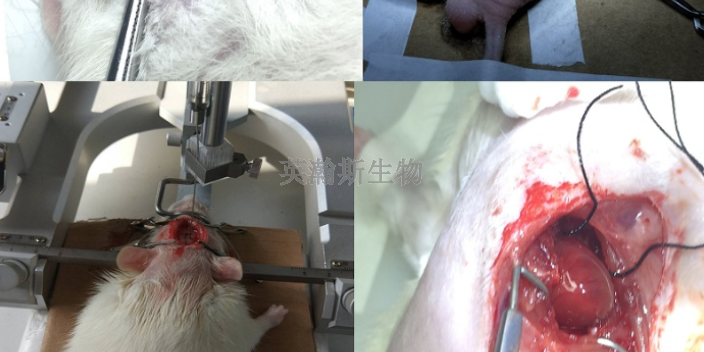
英瀚斯生物专做临床前动物实验。如果说异种移植已处在突破的“前夜”,那么猪胰岛移植***Ⅰ型糖尿病已成为实实在在的突破“前哨”。这一次,中国科学家走在了世界的前列。2002年国内科学家取得了进军异种移植后的***个重要突破:猪胰岛细胞经肝动脉移植***糖尿病在临床前动物试验中首先获得成功。当时,国际上普遍采用的是将胰岛通过肝脏的门静脉植入,但这种方法有时可能造成肝脏坏死,国内科学家创立的新方法使得手术安全性明显增加。1999年10月,在澳大利亚悉尼举行的第七届国际胰腺胰岛移植协会年会上,初次公布了动物实验的初步成果,该科学家的名字从此被国际移植医学界所熟知。
临床前动物实验到Ⅰ期临床试验——安全之路?——TGN1412Ⅰ期临床试验的惨痛教训的相关知识。2007年1月27日,来自英国伦敦帝国学院、伦敦国王学院和Babraham研究所的学者报告,人体的记忆T细胞可能是2006年3月造成抗CD28人源化单克隆抗体(TGN1412)Ⅰ期临床试验悲剧的原因。抗CD28人源化单克隆抗体——TGN1412Ⅰ期临床试验灾难性意外是2006年医药行业的热点新闻。对此,英国成立的单独**小组(ESG)曾召开过10多次会议,并于2006年12月7日发布了比较终研究报告。英国药物和保健品管理局(MHRA)也将于2007年2月6日召开研讨会以探讨从TGN1412事件中吸取的教训。对这一事件的回顾与分析无疑有助于人们更深入的思考药物试验面临的一些问题。英瀚斯是专业的中成药临床前动物实验外包公司。

从微生物产物中发现和研制抗*****,是极其复杂的、综合性极强的工作,被称为“一条龙”,大致可分为五部分:①获得产生菌:从全国各地采集的土壤样本中,培养、分离数以千计的菌株。②制备发酵液样品:将各种各样的菌种进行培养发酵,取得为数众多的发酵液样品。③初筛检测:对大量的发酵液样品进行筛选,检出有潜在抗**活性的样品。④提取纯化:对初筛阳性发酵液样品中的有效物质,进行提取与纯化。⑤临床前动物实验疗效评价:利用实验动物**模型,观察提取物的疗效。生物药临床前动物实验外包;辽宁比较好的临床前动物实验
化学药临床前动物实验多少钱?黑龙江专业临床前动物实验研究
临床前动物实验就在英瀚斯一站式实验中心。凡是没有经过院方伦理委员会的审核,一般是不合乎规范的。合乎规范也颇值得琢磨。有的是法律,有的是行政管理,有的是行业认可的标准,比如针对临床***的一些共识等。现在的问题是,没有一个统一的规范,也就很难定义违不违规了。对此,首先是要完善干细胞***的基础研究,踏踏实实完成从临床前动物实验到临床试验的过程,不可急功近利。同时,技术需要创新和尝试,由此带来的风险要靠严格的规范去控制,但不能因为害怕承担可能的风险,使规则的制定都停滞不前。黑龙江专业临床前动物实验研究