染方法大致可分为物理介导(如电穿孔法、显微注射和基因等)、化学介导(脂质体及其代替物、磷酸钙等)和生物介导(各类病毒,包括腺病毒、慢病毒、逆转录病毒、腺相关病毒等)三类途径。细胞转染又分为瞬时转染和稳定转染,瞬时转染是指外源基因进入受体细胞后,存在于游离的载体上,不整合到细胞的染色体上,基因表达维持时间较短,通常在96h以内;稳定转染是指DNA整合到宿主细胞的染色体中,使宿主细胞可长期表达目的基因。目前,大多采用依据不同质粒载体含有的抗性标志选用相应的对靶细胞进行筛选,常用的有嘌呤霉素(Puromycin)、G418(Geneticin)等。1、主要有下面几种化学法:磷酸钙法、DEAE-右旋糖苷法、阳离子脂质体法;物理法:电穿孔法、显微注射法、biolistic颗粒传递法;病毒介导法:逆转录病毒、腺病毒A.阳离子脂质体法:带正电的脂质体与核酸带负电的磷酸基团形成复合物被细胞内吞。特点:简单通用,适用性广,转染效率高,重复性好,但转染时需除血清,转染效率随细胞类型变化大。由于脂质体复合物与贴壁细胞的接触机会远大于悬浮细胞,所以贴壁比悬浮转染效率要高。悬浮细胞建议使用电穿孔法。B.电穿孔法:利用高压电脉冲对细胞膜的干扰。肝实质细胞体外常常被用作研究肝脏功能、能量代谢和肝脏疾病的良好模型。安徽非酒肝原代细胞分离培养评价
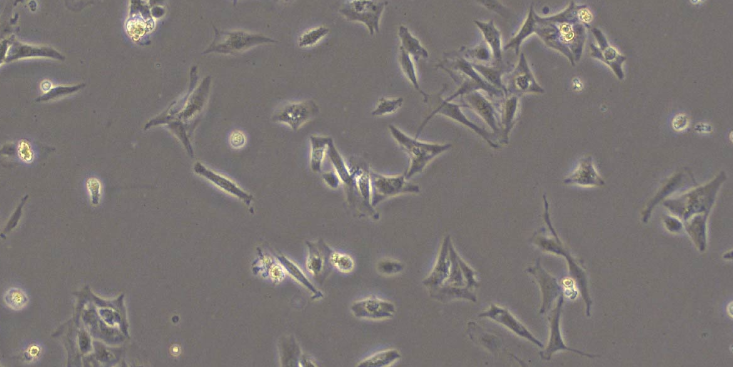
细胞凋亡与细胞坏死不同,细胞凋亡不是一件被动的过程,而是主动过程,它涉及一系列基因的ji活、表达以及调控等的作用,它并不是bing理条件下,自体损伤的一种现象,而是为更好地适应生存环境而主动争取的一种死亡过程。上海东寰为您分享细胞凋亡与细胞坏死的区别。细胞凋亡与程序性死亡其实从严格的词学意义上来说,细胞程序性死亡(PCD)与细胞凋亡是有很大区别的。细胞程序性死亡的概念是1956年提出的,PCD是个功能性概念,描述在一个多细胞生物体中某些细胞死亡是个体发育中的一个预定的,并受到严格程序把控的正常组成部分。例如蝌蚪变成青蛙,其bian态过程中尾部的消失伴随大量细胞死亡,高等哺乳类动物指间蹼的消失、颚融合、视网膜发育以及免yi系统的正常发育都必须有细胞死亡的参与。这些形的在机体发育过程中出现的细胞死亡有一个共同特征:即散在的、逐个地从正常组织中死亡和消失,机体无炎症反应,而且对整个机体的发育是有利和必须的。因此认为动物发育过程中存在的细胞程序性死亡是一个发育学概念,而细胞凋亡则是一个形态学的概念,描述一件有着一整套形态学特征的与坏死完全不同的细胞死亡形式。但是一般认为凋亡和程序性死亡两个概念可以交互使用。纤维化原代细胞分离培养厂家心肌的工作细胞包括心房肌和心室肌。心肌细胞为短柱状,一般只有一个细胞***肌细胞之间有闰盘结构。
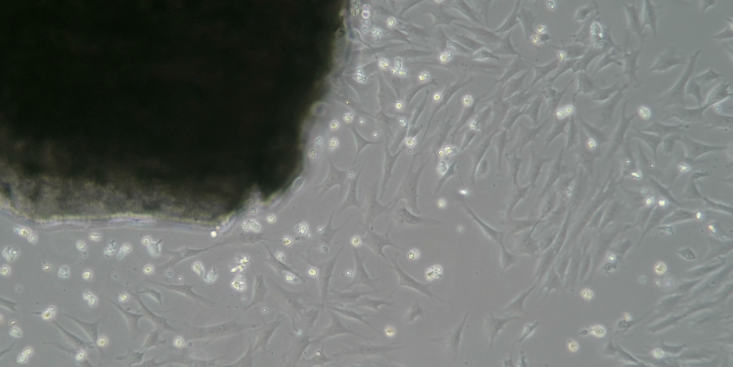
而且因为有5条定位线,与划痕相交,这样就有10个可固定监测点,不作重复,误差也很小。2、如果你连续监测24小时,你需要考虑到划痕缩小是细胞迁移和细胞繁殖共同作用的结果,而不是单纯的细胞迁移。如果你要单纯的考虑细胞迁移,你可以先用丝裂霉素(1ug/ml)处理一小时,抑制细胞的分裂,这样你的结果就是细胞迁移的作用了。另外,使用无血清培养基也可以降低增殖对实验结果的影响。3、照片拍完之后,可以用ImageJ来测量划痕区域的像素定量比较细胞迁移的速度。4、虽然无血清培养可以忽略细胞增殖的影响,但是由于细胞内信号传导系统整体性的下调节,细胞迁移的速度也会慢很多。5、应尽量清洗掉散落的细胞,对于一些细胞,低血清浓度下也能重新贴壁并增殖,此外也影响数据美观。四、常见问题1.划痕法测量适用的细胞范围较小,一般只适用于上皮细胞,纤维样细胞。2.虽然无血清培养可以忽略细胞增殖的影响,但是由于细胞内信号传导系统整体性的下调节,细胞迁移的速度也会慢很多。3、在用PBS缓冲液冲洗时,注意贴壁慢慢加入,以免冲散单层贴壁细胞,影响实验拍照结果。4、一般做划痕实验,需要排除细胞增殖的影响,一般在不影响细胞增殖的情况下采用低血清(<。
然后将感兴趣的药物通过电穿孔或脂质体转染等方法装入纯化的外泌体。外泌体内可装载的药物包括小分子化学药物、蛋白质和多肽、核酸药物、天然产物等。外泌体的抑制作用外泌体水平升高通常与不同类型的恶化相关,一些研究人员希望能通过降低外泌体到正常水平来防止不良预后。从这个角度出发,许多正在进行的研究旨在通过调节外泌体生成分泌的过程或通过特异性靶向其成分抑制其与靶细胞的相互作用来调节外泌体的产生。如今我们对外泌体机制和不同生理和病理条件下的功能的理解呈指数级增长,虽然目前其生物学功能还未完全解析清楚,但研究者们在许多领域均已对其进行了深入探索。外泌体不是废物颗粒,而是细胞间通讯的关键介质,作为宿主细胞的卫星,外泌体包含大量的生物信息,其功能超出了初的预期,宿主细胞控制着外泌体的内容物,从而改变了自己或其他细胞的命运。其次,外泌体对的进展和转移有着强烈的影响,可以通过外泌体预测转移的部位并建立转移前的生态位。参考文献:[1]高方园,焦丰龙,张养军,秦伟捷,钱小红.外泌体分离技术及其临床应用研究进展[J].色谱,2019,37。大鼠肺成纤维细胞分离自SD大鼠肺组织,多呈长梭形,具有突起,细胞胞体较大。
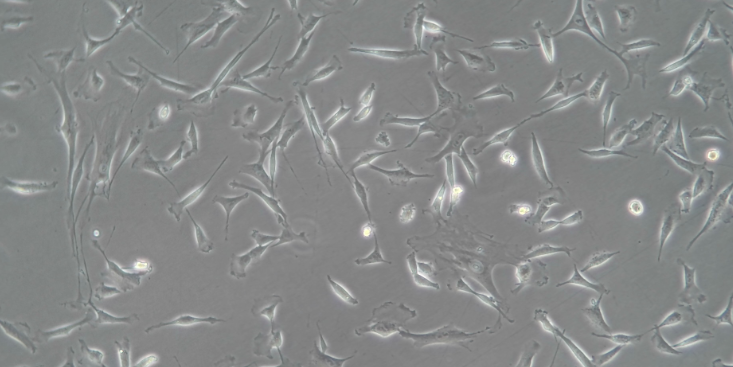
血管生成实验血管生成实验(DH0011)一、服务介绍应用Matrigel模拟机体环境,上面接种**细胞,观察血管生成情况。二、服务内容及价格服务编号服务内容服务价格服务周期(工作日)DH0011-1血管生成咨询咨询三、客户提供1.客户需提供生长状态良好的细胞株及相关处理药物2.实验前,客户需告知具体的细胞处理方式及详细要求。注:若有特殊处理的样品,请尽可能出示相关材料(具有保密性的材料除外)。四、服务流程1:细胞培养2:细胞转染或药物处理3:铺Matrigel胶4:接种细胞5:观察血管生成情况五、提交给客户结果1、完整实验报告2、细胞培养图片3、血管生成图片六、服务项目说明1.实验周期:具体需要根据细胞生长情况及实验内容而定。2.对实验有特殊要求,请另询价。3.双方签订合同后,收取50%首付后启动实验。提供的原代细胞均需经过细胞类型特异性标记物、细胞形态学以及微生物检测等服务的公司。青海哪家公司提供原代细胞分离培养评价
小鼠的肝细胞通常是指小鼠的肝实质细胞。安徽非酒肝原代细胞分离培养评价
建议按照2×106每孔的数量将293T细胞均匀铺入。(2)第二天:在24小时之内,观察293T细胞的汇合度在90%~95%之间时,向其中加入DNA-脂质体复合体,DNA-脂质体复合体制备方法如下:a)轻轻混匀LipoMax,根据说明书加入相应量于500µlOpti-MEM无血清培养基中,混合均匀并置于室温5分钟。b)在500µlOpti-MEM无血清培养基中稀释DNA,总质量为15µg按照载体质粒:psPAX2:=4:3:1的比例加入DNA。c)将稀释后的LipoMax和稀释后的DNA轻轻混匀,常温静置20分钟,形成DNA-LipoMax复合体。(3)将DNA-LipoMax复合体轻柔地滴加至细胞培养皿中,轻轻摇晃培养皿混匀,放入细胞培养箱中培养。(4)病毒收集浓缩病毒:加入DNA-LipoMax复合体48小时后,收集病毒上清,同时加入10ml预温的293T培养基到细胞培养皿中。将收集到的病毒上清存在4℃冰箱中;收集72小时病毒上清,与48小时病毒上清混在一起。将离心机温度降温到4℃,600g,离心5分钟,去除其中的细胞碎片,上清液经µm滤头过滤,加入病毒浓缩液,配制浓缩病毒液。将浓缩后的病毒放于4℃冰箱摇床上,旋转过夜。第二天,4度离心机,3000~4000g离心15分钟。弃掉上清液,加入1Xpbs或培养基重悬。安徽非酒肝原代细胞分离培养评价
上期我们主要讲解了细胞凋亡的早期检测方法,这期主要讲解一下细胞凋亡晚期中,核酸内切酶(某些Caspa...
【详情】也可以挑去单克隆细胞株进行进一步培养,以得到满意的稳定表达目的基因的细胞株。6)使用qRT-PCR和...
【详情】操作时戴合适的手套和安全眼镜并始终在化学通风橱里进行。(又称为二甲基亚砜)毒性级别:★★★实验场景:...
【详情】培养细胞不贴壁可能原因1.胰蛋白酶消化过度;2.支原体污染;3.培养基pH值过碱(NaHCO3分解)...
【详情】而且因为有5条定位线,与划痕相交,这样就有10个可固定监测点,不作重复,误差也很小。2、如果你连续监...
【详情】含血清完全培养液在2-8℃保存,需在1周内用完;5.增加接种细胞起始浓度;6.换用新的保种细胞;7....
【详情】把培养瓶置于倒置显微镜下观察,如大部分细胞变圆,立即移除胰酶消化液(如大部分细胞飘起,可不移除胰酶消...
【详情】注意事项1.病毒包装的几个关键点主要包括:细胞因素、载体系统(尽量使用成熟的商业化载体系统)、构建重...
【详情】注意事项1.病毒包装的几个关键点主要包括:细胞因素、载体系统(尽量使用成熟的商业化载体系统)、构建重...
【详情】细胞增殖通俗点讲,细胞增殖也就是细胞分裂,就像我们每个人的生命起点都是由一个受精卵不断的分裂而来,然...
【详情】细胞迁移和侵袭实验细胞迁移和侵袭技术服务(DH0004)一、服务介绍细胞迁移\侵袭是指细胞在接收到信...
【详情】防止有Matrigel流经上孔而留下残留胶;3、需要按照细胞的生长速度定时采集图像,并且对其成管长度...
【详情】